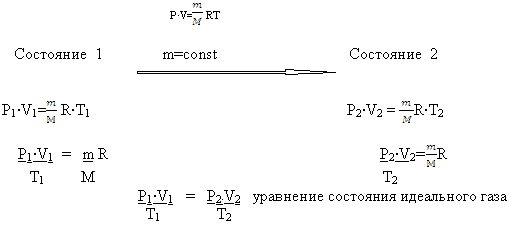
Как называется уравнение состояния идеального газа

2.5. Универсальное уравнение состояния идеального газа
Уравнение состояния идеального газа иногда уравнение Клапейрона или уравнение Менделеева — Клапейрона — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:. Так как , где —количество вещества, а , где — масса, —молярная масса, уравнение состояния можно записать:. Последнее уравнение называют объединённым газовым законом. А в форме пропорции этот закон удобен для расчёта перевода газа из одного состояния в другое.



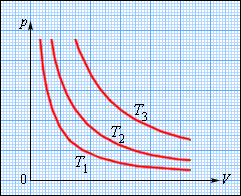




Газы часто используются в тепловых двигателях в качестве рабочего тела. Это обусловлено их свойством менять объем в широком диапазоне, и, следовательно, получать работу расширения. Знать свойства газов очень важно, так как необходимо анализировать процессы, проходящие с рабочим телом в установках и выбирать наиболее экономичные схемы циклы этих установок. Изучение свойств газов ведется двумя путями: экспериментальным и теоретическим. На начальной стадии изучения свойств газов преобладали экспериментальные исследования.
- Уравнение состояния идеального газа
- Здесь, конечно, речь идёт только о газе, находящемся в состоянии термодинамического равновесия , которое означает, что все макроскопические параметры не изменяются со временем. Несколько слов о равновесных процессах.
- Идеальным газом называется такой газ , у которого отсутствуют силы взаимного притяжения и отталкивания между молекулами и пренебрегают размерами молекул. Все реальные газы при высоких температурах и малых давлениях можно практически считать как идеальные газы.
- Они взаимодействуют со стенками сосуда посредствам упругих соударений. Применим неравенства:.
- CSS adjustments for Marinelli theme
- Регистрация Вход. Ответы Mail.
- Уравнение состояния идеального газа. Уравнением состояния называется уравнение, связывающее параметры физической системы и однозначно определяющее ее состояние.
- Удобная навигация, видео-разборы тем, задачи для самопроверки — всё это в вашем кармане. А ещё раздел с полезными материалами, календарь занятий и уведомления о предстоящих уроках.





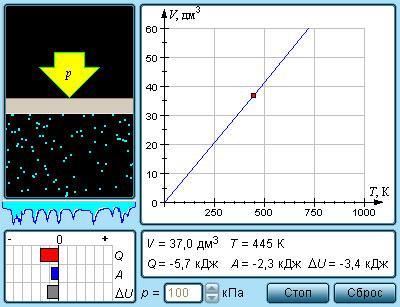


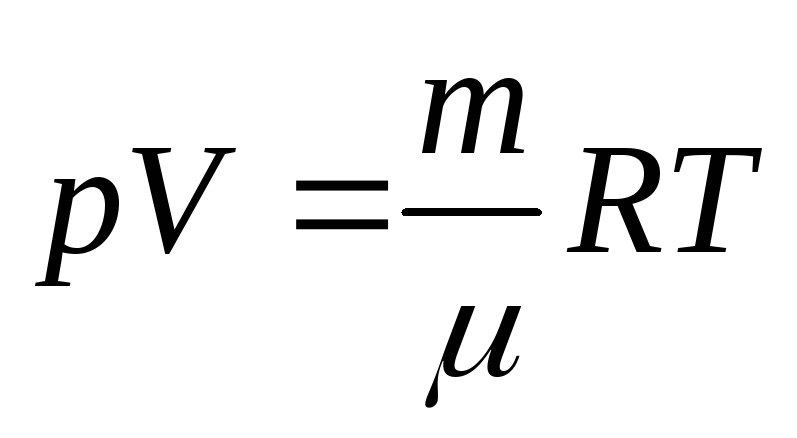
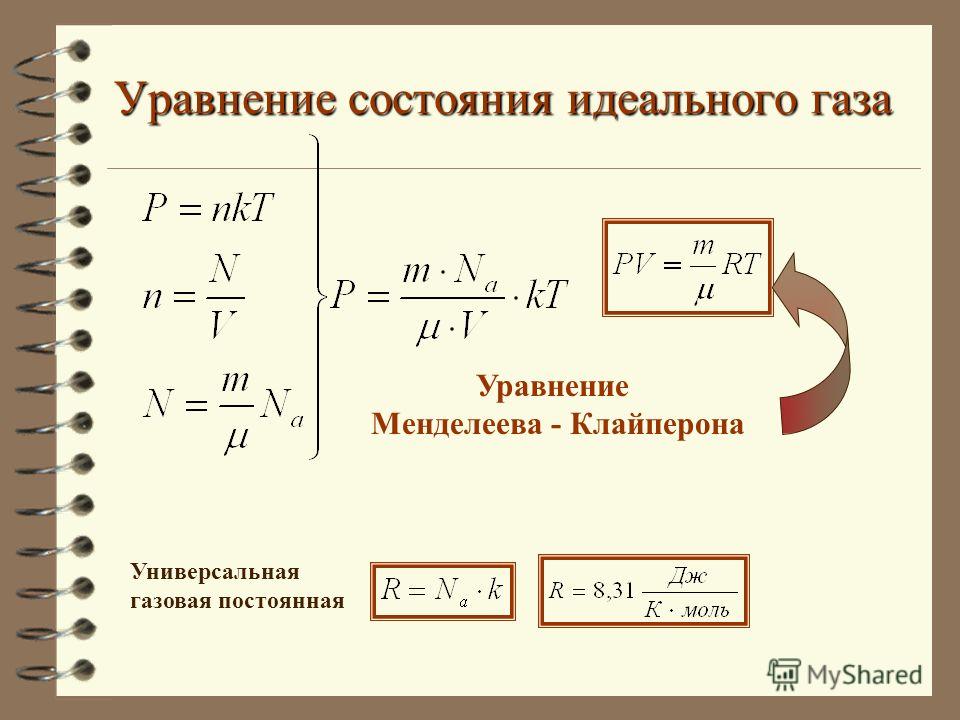
Для этого нужно использовать равенства. Здесь N — число молекул в сосуде, N А — постоянная Авогадро, m — масса газа в сосуде, M — молярная масса газа. В итоге получим:. Произведение постоянной Авогадро N А на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. Это утверждение называется законом Авогадро.